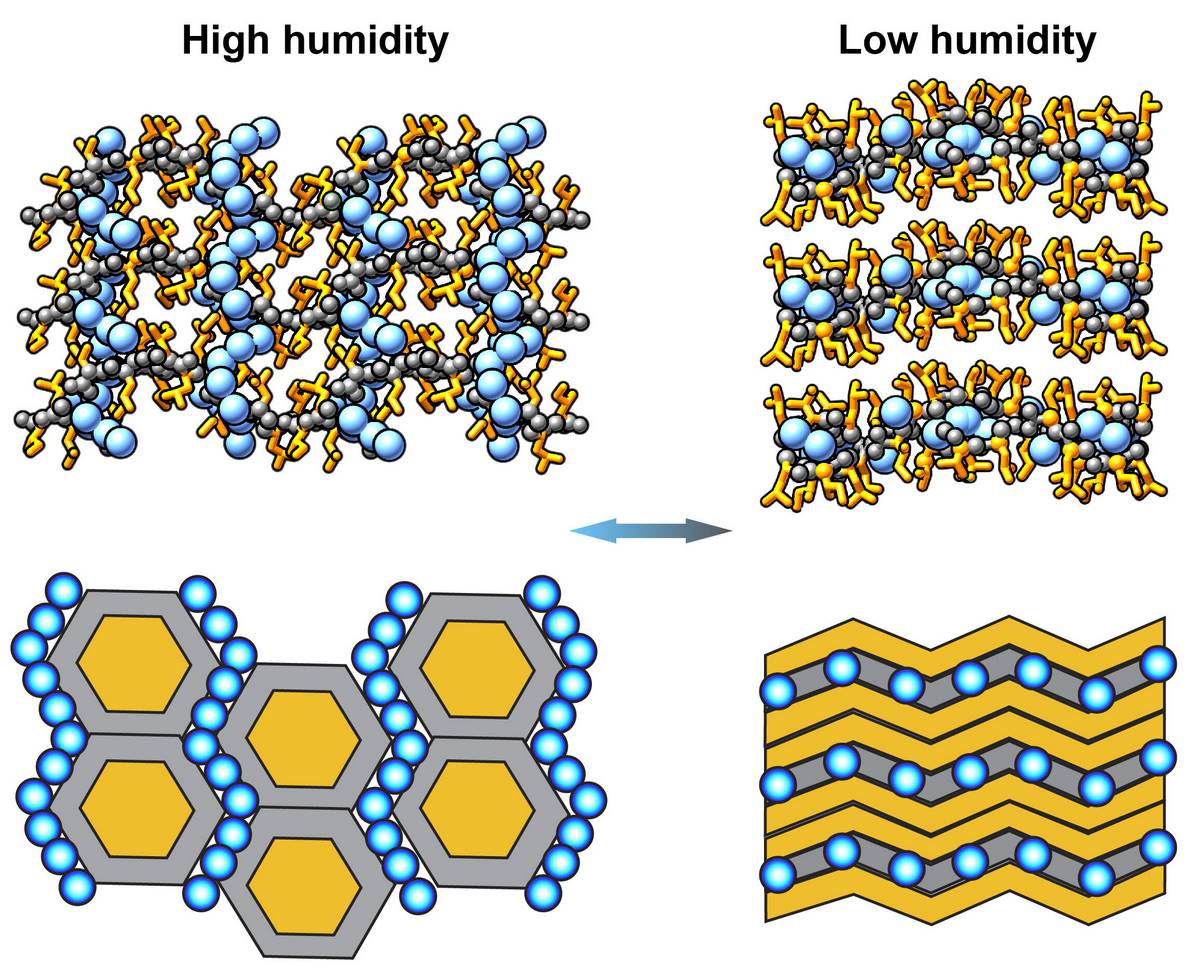
Уявіть тверде тіло, яке перебудовує свою внутрішню молекулярну архітектуру в буквальному сенсі від того, що на нього дихнути. Саме такий матеріал створили дослідники з Центру передових наукових досліджень CUNY ASRC — і він описаний у свіжій статті журналу Matter. Кристалічні тверді речовини на основі пептидів можуть повністю змінювати свою упаковку у відповідь на найменші зміни вологості, зберігаючи при цьому цілісність і механічну міцність.
Що відомо коротко
- Пептидні кристали оборотно перебудовують усю молекулярну архітектуру — від жорсткої шільникової до м’якої шаруватої структури та назад
- Трансформацію запускає проста зміна вологості, без рідкої води, підігріву або хімічних реагентів
- Це перший у світі зафіксований швидкий твердотільний перехід між шаруватою структурою Ван-дер-Ваальса та гексагональною упаковкою
- Вода в кристалі відіграє роль не пасивного наповнювача, а структурного компонента і джерела енергії
- Матеріал відкриває шлях до дешевих адаптивних пристроїв: оптичних, медичних, робототехнічних
Чому більшість матеріалів «застигають» раз і назавжди
Сталь, пластик, кераміка — всі ці матеріали проектуються з фіксованими властивостями: жорсткими або гнучкими, міцними або легкими. Їхні молекули займають певне положення під час виготовлення й більше практично не рухаються. Така стабільність — велика перевага, але й суттєве обмеження: матеріал не може адаптуватися до змін довкілля.
У живих системах все інакше. Білки постійно змінюють форму у відповідь на сигнали оточення — температуру, кислотність, вологість, присутність інших молекул. Саме ця динамічна перебудова дозволяє ферментам каталізувати реакції, рецепторам впізнавати сигнали, а м’язам скорочуватися. Відтворити таку поведінку в синтетичних твердих тілах науковці намагалися десятиліттями.
Амінокислоти як будівельний набір
Дослідники під керівництвом Сі Чена (CUNY ASRC та Міський коледж Нью-Йорка) і Рейна Улійна (засновник Ініціативи CUNY ASRC Nanoscience) вирішили не імітувати цілі білки — занадто складна задача. Натомість вони використали найпростіші молекулярні будівельні блоки білків — амінокислоти — як хімічний «конструктор» для дизайну матеріалів.
Із коротких ланцюжків амінокислот — пептидів — команда синтезувала кристалічні структури з особливою властивістю: обмежена кількість молекул води, замкнених всередині пор, може перерозподілятися між різними ділянками кристала, змінюючи баланс сил між молекулами.
«Природа показує нам, що стабільність та адаптивність не обов’язково мають бути протилежностями», — сказав Сі Чен. «Білки, як правило, досить стабільні, але можуть адаптувати свою форму до місцевих умов. Нашою метою було втілити цей самий принцип у твердотільних матеріалах».
Перше у світі швидке твердотільне перетворення
Ключовий результат роботи — демонстрація першого у світі швидкого твердотільного перетворення між двома топологічно різними кристалічними структурами: шаруватою, м’якою структурою Ван-дер-Ваальса та дуже жорсткою, гексагонально упакованою архітектурою. Перехід відбувається без руйнування кристала.
Перший автор роботи, Вігнеш Атхіярат, так описав масштаб змін: «Це не дрібні зміни чи легкі дихальні рухи. Матеріал повністю реорганізує упаковку своїх молекул. Такий вид перетворення надзвичайно рідкісний у твердотільних системах».
Оскільки внутрішня топологія визначає механічні та оптичні властивості матеріалу, такі структурні переходи призводять до значних, контрольованих змін жорсткості, пружності й характеру взаємодії матеріалу зі світлом.
Вода як двигун трансформації
Ключем до всього є роль обмеженої води в порах кристала. Замість того щоб бути пасивним наповнювачем, молекули води виступають одночасно як структурний компонент (стабілізують певну конформацію) і як джерело енергії (перерозподіляючись, забезпечують перехід між станами).
Рейн Улійн акцентував на принциповій відмінності від попередніх підходів: «Особливо захоплює те, що ми змогли досягти динамічної реконфігурації у твердому стані — тобто без наявності рідкої води. З білками цього важко досягти».
На відміну від більшості «адаптивних» матеріалів, які здатні лише трохи розширюватись або стискатись, нові пептидні кристали перемикаються між принципово різними режимами упаковки — наче повністю змінюють свою внутрішню анатомію.
Чому це важливо для науки і технологій
Матеріали, які адаптуються до умов навколишнього середовища, потрібні в багатьох сферах. Сенсори, гнучкі дисплеї, розумні протези, м’яка робототехніка, адаптивні фільтри, оптичні перемикачі — скрізь виграшним був би матеріал, здатний «вирішувати», яким йому бути.
Досі більшість таких розробок стикалась із суперечністю: матеріали або стабільні, але негнучкі, або адаптивні, але крихкі. Нові пептидні тверді речовини долають цей розрив: вони одночасно стабільні й адаптивні.
Подібний принцип адаптивності до середовища вже давно захоплює дослідників у біологічному контексті. Наприклад, секрет неймовірної міцності павутини дарвінівських павуків також криється у білкових молекулах із динамічними структурними блоками. Нові пептидні матеріали — це спроба перенести подібні принципи у синтетичний твердотільний світ.
Важливо й економічне значення: прості амінокислоти є дешевою, добре відомою сировиною. Це знижує вартість виробництва та відкриває шлях до масштабованого виготовлення адаптивних матеріалів — що досі було критичним бар’єром на шляху від лабораторії до реального застосування.
Досягнення паралельно перегукується з іншими проривами у матеріалознавстві: наприклад, вчені вже створили перший у світі напівпровідник з графену — матеріалу, чиї властивості визначаються не хімічним складом, а архітектурою структури. В обох випадках головна ідея однакова: геометрія — це властивість.
Цікаві факти
- Звичайний кристал за визначенням має жорстко фіксовану решітку — тому тверде тіло, що повністю перебудовує свою упаковку без розчинення, є науковою аномалією
- Перехід між структурами в нових матеріалах запускається зміною відносної вологості приблизно на 10–20% — менше, ніж різниця між сухим і вологим повітрям приміщення
- Пептиди — це «скорочені копії» білків: якщо типовий білок налічує сотні амінокислот, пептид може складатися лише з двох–десяти
- У медицині вже тестують пептидні матеріали для імплантів, що адаптуються до тканин пацієнта замість того, щоб викликати запальну реакцію
- Дослідницька група CUNY ASRC об’єднала фахівців з кількох країн — міжнародна кооперація є стандартом для такого роду прикордонних наукових проектів
FAQ
Як саме вологість може змінити жорсткість твердого тіла? Молекули води, замкнені в порах кристала, взаємодіють з амінокислотними ланцюжками через водневі зв’язки й сили Ван-дер-Ваальса. Коли їх кількість змінюється (через зміну вологості повітря), баланс сил між молекулами зрушується: одна конфігурація стає енергетично невигідною, і кристал перебудовується у нову стабільну форму. Важливо, що цей процес оборотний — кристал повертається до вихідного стану, якщо умови змінюються назад.
Чи можна застосувати такі матеріали в медицині вже зараз? Поки що ні — дослідження перебуває на фундаментальному рівні. Але принципові перешкоди знято: матеріал нетоксичний (складається з природних амінокислот), стабільний при механічних навантаженнях і виготовляється з доступної сировини. Наступні кроки — масштабування синтезу та відпрацювання конкретних застосувань.
Чому попередні адаптивні матеріали не могли зробити те саме? Більшість відомих адаптивних матеріалів — гелі, гідрогелі, рідкі кристали — або вимагають рідкої фази (не є справжніми твердими тілами), або здатні лише на невелике розширення/стиснення, не змінюючи топологію структури. Тверді тіла ж традиційно вважалися «закритими» для такої реорганізації через жорсткість кристалічної решітки.
Тверді матеріали навчили перебудовуватись, як живі білки з’явилася спочатку на Цікавості.


 1981
1981